Teplota u dětí dovede stoupat velmi rychle, proto je třeba reagovat na teplotu a bolest včas. Při zvýšené teplotě u dětí vyzkoušejte sirupy a čípky.
Léčivý přípravek

Na snížení horečky a na mírné až středně těžké bolesti hlavy, bolesti…
159 Kč
Léčivý přípravek

Ke krátkodobé léčbě horečky, včetně horečky po očkování, mírných až…
225 Kč
Léčivý přípravek
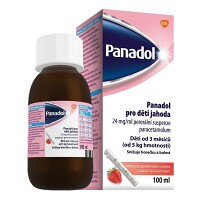
Suspenze pro děti ke snížení horečky a bolesti s jahodovou příchutí.…
149 Kč
Léčivý přípravek
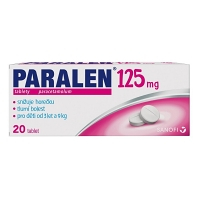
Tablety se podávají dětem od 3 let a 9 kg ke snížení zvýšené tělesné…
38 Kč
Léčivý přípravek

Ke krátkodobé léčbě horečky, včetně horečky po očkování, mírných až…
229 Kč
Léčivý přípravek

Ke snížení horečky, k tlumení mírných až středně těžkých bolestí…
162 Kč 155 Kč -4 %
Léčivý přípravek

Snižuje horečku, tlumí mírné až středně silné bolesti hlavy, zubů…
176 Kč 155 Kč -12 %
Léčivý přípravek

Léčí krátkodobě horečku (včetně horečky po očkování) a tlumí mírnou…
275 Kč 249 Kč -9 %
Léčivý přípravek

Panadol Baby čípky je určen ke snížení horečky provázející chřipku,…
99 Kč 89 Kč -10 %
Léčivý přípravek
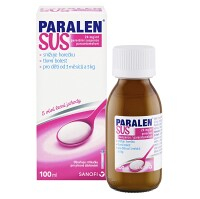
Podává se dětem od kojeneckého věku ke snížení horečky při…
135 Kč
Léčivý přípravek

Snižuje horečku, tlumí mírné až středně silné bolesti hlavy, zubů…
249 Kč
Léčivý přípravek

Ke snížení horečky, k tlumení mírných až středně těžkých bolestí…
112 Kč 109 Kč -3 %
Léčivý přípravek

Přípravek zmírňuje příznaky chřipky, nachlazení, snižuje horečku a má…
199 Kč 183 Kč -8 %
Léčivý přípravek

Ke snížení horečky, k tlumení mírných až středně těžkých bolestí…
85 Kč
Homeopatický lék
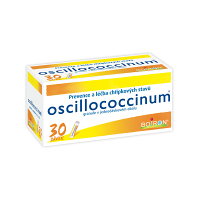
Uživaný k prevenci a léčbě chřipkových stavů.
579 Kč 549 Kč -5 %
Léčivý přípravek
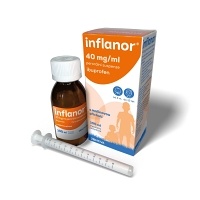
Přípravek je určen ke krátkodobé léčbě příznaků mírné až středně…
189 Kč 169 Kč -11 %
Léčivý přípravek

Panadol pro snížení horečky a úlevu od bolesti pro děti od 15 kg.…
96 Kč 89 Kč -7 %
Léčivý přípravek

Brufen obsahuje léčivou látku ibuprofen, která snižuje horečku a…
125 Kč 111 Kč -11 %
Léčivý přípravek
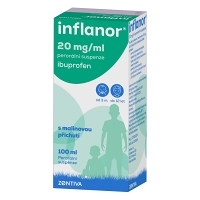
Přípravek je určen ke krátkodobé léčbě příznaků mírné až středně…
125 Kč 109 Kč -13 %
Homeopatický lék

Homeopatický lék, který se tradičně používá při podpůrné léčbě…
199 Kč 169 Kč -15 %
Léčivý přípravek

Tlumí bolest, snižuje horečku a zmírňuje zánět různého původu pro…
169 Kč 138 Kč -18 %
Léčivý přípravek
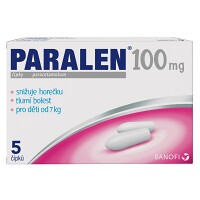
Snižuje horečku při chřipkových onemocněních, vhodný jako doplňková…
41 Kč 40 Kč -2 %
Léčivý přípravek

Rychle a účinně zmírní příznaky chřipky a nachlazení dítěte, sníží…
129 Kč
Stav, když má ditě zvýšenou teplotu v rozsahu 37,5 °C - 38,5 °C označeujem jako teplota, horečka nastává v okamžiku, když je hranice 38,5 °C převýšena. Příčin vedoucí k těmto stavům je mnoho. Může se jednat o virové onemocnění, reakci po očkování, porucha obranyschopnosti nebo následek úrazových stavů či jiných onemocnění.
Pokud horečky přetrvávají vyhledejte vždy obratem pomoc lékaře. Vysoké teploty mohou mít za následek křeče, vyvolávající epileptické záchvaty.
Na trhu s léčivy naleznete širokou nabídku přípravků, které působí na zvýšenou teplotu. Tyto produkty lze rozlišit na sirupy, tablety nebo čípky, dále se výrobky liší podle obsažené látky, nebo značky- např. Panadol. Před požitím léků vždy čtěte příbalovou informaci nebo se poraďte o dávkování s odborníkem.
Kategorii Léky na teplotu u dětí najdete i na našem slovenském e-shopu MojaLekáreň.sk
Teplota u dětí dovede stoupat velmi rychle, proto je třeba reagovat na teplotu a bolest včas. Při zvýšené teplotě u dětí vyzkoušejte sirupy a čípky.
Stav, když má ditě zvýšenou teplotu v rozsahu 37,5 °C - 38,5 °C označeujem jako teplota, horečka nastává v okamžiku, když je hranice 38,5 °C převýšena. Příčin vedoucí k těmto stavům je mnoho. Může se jednat o virové onemocnění, reakci po očkování, porucha obranyschopnosti nebo následek úrazových stavů či jiných onemocnění.
Pokud horečky přetrvávají vyhledejte vždy obratem pomoc lékaře. Vysoké teploty mohou mít za následek křeče, vyvolávající epileptické záchvaty.
Na trhu s léčivy naleznete širokou nabídku přípravků, které působí na zvýšenou teplotu. Tyto produkty lze rozlišit na sirupy, tablety nebo čípky, dále se výrobky liší podle obsažené látky, nebo značky- např. Panadol. Před požitím léků vždy čtěte příbalovou informaci nebo se poraďte o dávkování s odborníkem.
Kategorii Léky na teplotu u dětí najdete i na našem slovenském e-shopu MojaLekáreň.sk
Nejdříve se musíte přihlásit.